Nanostruttura biomimetica: la natura come modello
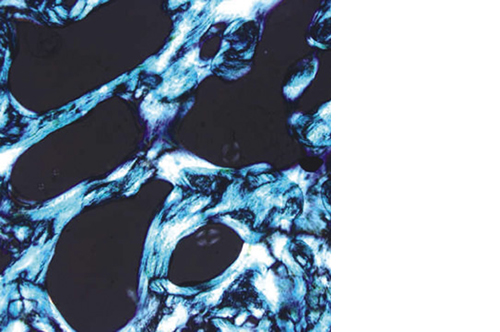
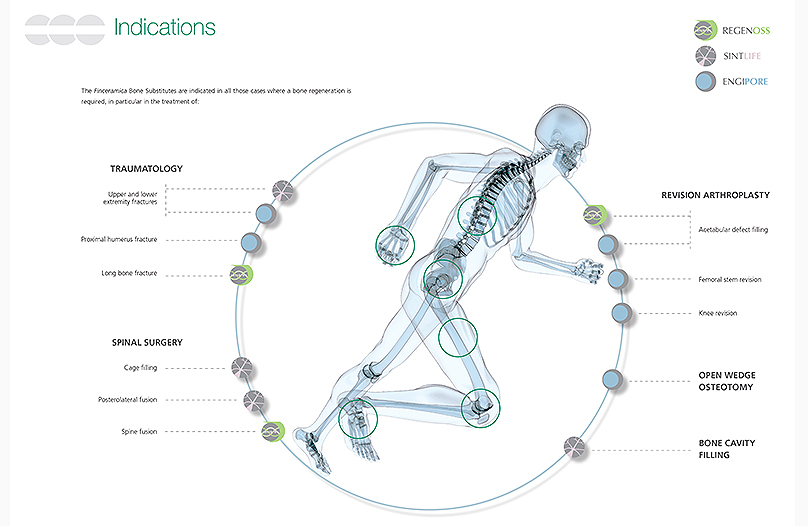
RegenOss è uno scaffold totalmente biomimetico: la sua peculiare struttura e la sua composizione chimica conferiscono al prodotto caratteristiche del tutto simili all’osso umano.
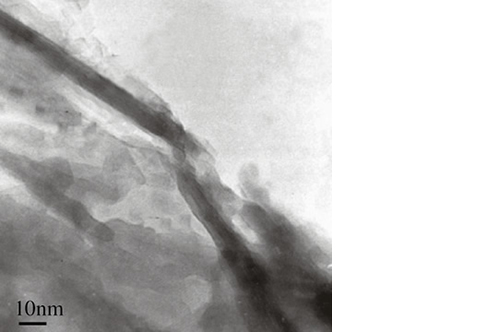
RegenOss è prodotto attraverso un esclusivo processo, brevettato a livello mondiale, di enucleazione di nanocristalli di magnesio-idrossiapatite nelle fibre di collagene. Il processo imita ciò che avviene in natura durante la fase di neoossificazione.
Rigenerazione guidata
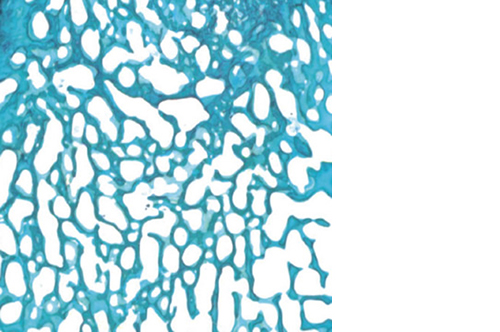
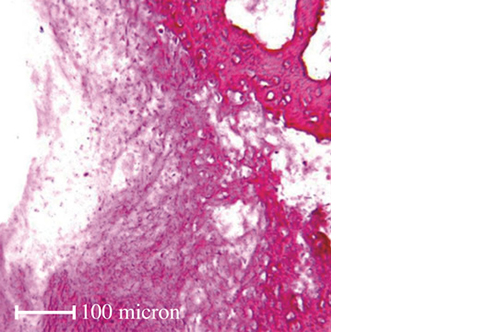
Grazie alla elevata idrofilicità, RegenOss è in grado di assorbire rapidamente i fluidi biologici, le molecole e le cellule che promuovono la rigenerazione ossea. La sua architettura favorisce l’adesione e la proliferazione cellulare.
RegenOss viene gradualmente degradato dall’azione enzimatica e cellulare in un tempo fisiologicamente adeguato (6-12 mesi), rimanendo in situ per il tempo necessario per “guidare tridimensionalmente” la deposizione del nuovo tessuto osseo.